|
牛瘟實驗室診斷標準操作程序(以下簡稱本標準)所制訂之內容係提供於實驗室處理相關病材,進行牛瘟實驗室診斷操作時所必須之程序,以確保檢驗水準之一致。 |
| |
| 1. |
牛瘟病毒: |
| |
屬於副黏液病毒科 (paramyxoviridae) 的痲疹病毒(morbillivirus),可造成家用牛及水牛的急性及致死性的疾病,綿羊、山羊、豬、野豬及野生反芻獸等也可被傳染。本病的臨床特徵是發燒,在齒齦、舌尖、頰及硬顎等處會發生漸進性糜爛,並伴有漿液性及黏液膿性的眼鼻分泌物,消化道則明顯的發生嚴重性下痢。典型的牛瘟病死牛隻的特色是脫水、瘦弱、髒污及有惡臭。鼻子和頰帶有黏液膿性分泌物的痕跡,眼睛凹陷及結膜充血。在口腔經常有廣大的壞死上皮脫落,而且與鄰近健康的黏膜區有很明顯的界限。 |
|
| |
| (1) |
實驗室:符合國家安全標準III級實驗室 |
| (2) |
高速離心機:Kubota 1300 |
| (3) |
離心機:Jouan C412 |
| (4) |
桌上小型離心機:KM-15200, Kubota |
| (5) |
顯微鏡:Zeiss, Germany |
| (6) |
恆溫箱:SHEL LAB model TC2323 |
| (7) |
水浴槽:Hotech, water bath 810 |
| (8) |
兔化牛瘟病毒株:LA AKO 株,分讓自日本農林省家畜衛生試驗場 |
| (9) |
磷酸緩衝食鹽溶液:
| NaCl |
(Merck) |
8.0 |
gm |
| KCl |
(Merck) |
0.2 |
gm |
| Na2HPO4.7H2O |
(Merck) |
2.172 |
gm |
| KH2PO4 |
(Merck) |
0.2 |
gm |
| 加蒸餾水至 |
|
1,000 |
mL |
以121 ℃ 15 lb / cm2高壓滅菌20分鐘。並以T.S.A. Agar 作無菌檢定。 |
| (10) |
細胞培養液:
每包 1 公升裝 MEM 鹽基粉末(Gibco) 加入滅菌再製蒸餾水至 1 公升。經溶解後加入 2.3 gm 的 NaHCO3,以 0.22μM Millipore 過濾並分裝於 500 mL血清瓶內,TSA Agar無菌檢定通過後放入 4 ℃ 冰箱保存備用。 |
| (11) |
細胞生長液:
每100 mL MEM 細胞培養液內加入8 mL 胎牛血清 (8 %) 及抗生素 (penicillin 100 U / mL和streptomycin 100μg/ mL),供細胞增殖培養用。 |
| (12) |
細胞維持液:
係於每 100 mL MEM 細胞培養液內加入 2 mL 胎牛血清 (2%) 及抗生素(同細胞生長液),供細胞維持用。 |
|
| |
| 1. |
對高熱期之動物,可用10 國際單位/毫升 (IU/Ml) 的肝素或0.5 mg / mL的EDTA等抗凝劑採取其抗凝的全血,以進行白血球培養,樣品需與抗凝劑完全混合不可以冷凍,可用冰鎮傳送至實驗室。到達實驗室後,將抗凝血以2,500 g離心15分鐘使在血漿與紅血球之間產生血塊黃層 (buffy coat),儘可能將此層取乾淨,與20 mL生理食鹽水混合後依據清洗步驟再離心,以洗去血漿中的任何中和抗體,得到的細胞沉澱物,以細胞培養維持液泡成懸浮液,即可用來分離病毒。 |
| |
|
| 2. |
對於死亡的動物,在屍體解剖時採取脾臟或肩胛前淋巴結或腸繫膜淋巴結以供病毒分離,這些樣品可以冷卻至零下溫度,並迅速送到實驗室。到達實驗室後,將剖檢採集的臟器先在無血清的培養維持液中以標準的磨碎或剝取技術來軟化,並以細胞培養液做成 20% 淋巴結或脾臟的懸浮液,再以 750 xg 離心 10 分鐘,這些樣品的上清液即可用來分離病毒。 |
| |
|
| 3. |
對於牛隻感染牛瘟的鑑定,尚可在發病初期或口腔黏膜糜爛期時用綿花棒在靠近上下眼瞼處採取感染牛隻的眼睛分泌物,以供牛瘟抗原沉澱反應。 |
|
| |
| 1. |
株化細胞分離病毒與同定:
| (1) |
病毒分離之診斷是以上述病材接種繼代細胞如:B95a小猿類淋巴胚細胞或初代小牛腎臟細胞或非洲綠猴腎臟(VERO) 細胞等均可適用。細胞可用角瓶等培養,培養的方式是細胞以6孔組織培養盤增殖成單層細胞後,再接種1~2 mL的病材液進行吸著反應1小時。 |
| (2) |
以PBS洗滌後然後再加入細胞維持液 3 mL,置入37℃,5% CO2 恆溫箱中培養。每天以顯微鏡觀察細胞病變作用 (CPE) 的發生,若有病毒感染者通常3天內會有CPE,其特徵為折射 (refractility)、細胞圓形化 (cell rounding)、細胞的延長細胞質橋(星狀細胞)回縮或形成融合細胞。可取病毒液進行電子顯微鏡檢查有無病毒顆粒,也可以痲疹病毒特異性沉澱抗原之存在或使用結合單源抗體 (MAb) 進行特異性免疫螢光抗體反應的証明而得以確認牛瘟病毒。 |
| (3) |
若 5 天仍無 CPE 則須再繼代,而以第一代培養細胞經冷凍解凍、離心後,上清液用來繼續接種新的單層細胞。並以 (2) 之方法進行觀察與鑑定。 |
|
| |
|
| 2. |
從白血球分離病毒:
| (1) |
以 20 mL 注射針筒吸取 100 國際單位 (IU) 的肝素或 5 mg 的 EDTA 等抗凝劑對高熱期之動物,採取 10 mL 的抗凝血,使血液與抗凝劑完全混合均勻,以冰鎮傳送至實驗室。 |
| (2) |
到達實驗室後,將抗凝血注入 15 mL 離心管中,另備一支離心管與之平衡後,對稱放入離心機內,以 4 ℃ 2,500 xg 離心 15 分鐘,待離心機靜止後,小心取出離心管(不可搖動內液)置於架上,此時可見血漿與紅血球之間已產生血塊黃層 (buffy coat)。 |
| (3) |
將長針接在 10 mL 針筒上,背向光源,將長針穿過血清層深入至血塊黃層表面,沿著該層面,輕輕將該層吸取至針筒中(需儘可能將此層取乾淨,並避免取到太多之血球),再將針筒內液注入裝有 20 mL 生理食鹽水之 50 mL 離心管中,充分混合均勻後再以 (2) 之條件離心,重複 (3) 及 (2) 之步驟二次,以洗去血漿中的任何中和抗體。最後一次離心得到的細胞沉澱物,再以 1 mL 細胞培養維持液泡成懸浮液,即可用來分離病毒。 |
| (4) |
用6孔組織培養盤培養單層的感受性細胞,每孔接種 0.2 mL 之白血球懸浮液,於 37℃ 5% CO2 培養箱中感作1小時,其間每隔 8-10 分鐘須將 6 孔組織培養盤搖晃一次,使細胞均有液體滋潤,以防細胞因乾燥而死亡。 |
| (5) |
感作終了時,每孔再加入 3 mL 維持液,即可送入 37℃ 5% CO2 培養箱中,進行病毒分離。 |
| (6) |
本試驗必須無菌操作,並需含有 RPV 陰性與陽性的對照,但必需非常小心不可污染到正常的試驗。例如可最後才操作陽性對照,並且使用不同的細胞培養盤。 |
| (7) |
顯微鏡下每天觀察是否有CPE,若有CPE,則再做特異性抗原沉澱或特異性免疫螢光抗體反應來確認。 |
| (8) |
若5天仍無CPE則須再繼代,而以第一代培養細胞經冷凍解凍、離心後,上清液用來繼續接種新的單層細胞。並以 (7) 之方法進行觀察與鑑定。 |
|
| |
|
| 3. |
從淋巴結或脾臟分離病毒:
| (1) |
取 2 g之淋巴結或脾臟組織置於揅缽中,以杵揅磨成乳狀,加入 8 mL 之細胞培養液,充分磨勻後,將揅磨液裝入 15 mL 離心管中,另備平衡用離心管,對稱放入離心機中,以4℃ 2,500 xg 離心 15 分鐘,待離心機靜止後,小心取出離心管(不可搖動內液)置於架上,即完成 20% 組織乳劑之製作。 |
| (2) |
取上述製備完成之 20% 組織乳劑上層液,供作病毒分離,並依前述白血球分離病毒之第 (5) 步驟,以 0.2 mL乳劑接種細胞及進行感作。 |
| (3) |
感作終了時,以3 mL維持液將每孔之單層細胞洗2次後,即可依前述白血球分離病毒之第 (6) 至 (8) 步驟,進行觀察及鑑定是否有牛瘟病毒。 |
|
| |
|
| 4. |
牛瘟及小反芻獸瘟疫的區別: |
| |
臨床的觀察與沉澱抗原檢測試驗是無法區別牛瘟及小反芻獸瘟疫,在同時存在有這二種疾病的國家,對於綿羊或山羊的所有類似牛瘟的爆發,都必須施行區別這二種疾病的檢測。
| (1) |
差別的免疫捕捉: |
| |
以一種可以直接對抗此二種病毒的N蛋白的單源抗體,作為捕捉抗體 (capture antibody),而以第二種標有生物素 (biotin) 分別對牛瘟病毒或小反芻獸瘟疫病毒特異之單源抗體,用來決定是捕捉到該二種病毒中之那一種病毒的N蛋白。 |
| |
操作方法如下:
| (A) |
取96 孔平底微量盤 (96 wells microplate),每孔加入100 μL的捕捉抗體被覆溶液,輕輕敲打微量盤的邊緣,以確定抗體均完全分佈在每個孔洞的底部,將盤子密封之後,再將其放入4 ℃ 冷房的定軌搖擺器上作用一個晚上 (overnight) 或是在 37 ℃ 暖房的定軌搖擺器上作用1小時。 |
| (B) |
甩掉孔洞中之被覆溶液後,以pH7.4的0.002 M PBS清洗每個孔洞三次,甩乾之後,每孔加入50μL的測試樣品(先以溶解緩衝液作十倍稀釋)、25μL的指示劑單源抗體稀釋液(小反芻獸瘟疫稀釋一千倍;牛瘟稀釋五百倍)及25μL 的鏈狀抗生物素-過氧化氫(streptavidin-peroxidase)(最後稀釋成三千倍),然後將這些盤子放在 37 ℃ 暖房的定軌搖擺器 (orbital shaker) 上作用1小時。 |
| (C) |
甩掉孔洞中之測試溶液後,以pH7.4的0.002 M PBS清洗每個孔洞三次,甩乾之後,再加入100μL的正-酚基二氨 (ortho-phenylenediamine),在室溫作用 10 分鐘後,加入100μL的1N硫酸終止反應。 |
| (D) |
以ELISA自動判讀機用492 nm波長所讀取的吸光值,判讀結果。這個測試可用來確定野外樣品或生長在組織培養中的病毒是牛瘟或是小反芻獸瘟疫病毒。 |
|
| |
|
| (2) |
聚合酶鏈反應: |
| |
已開發一種反轉錄聚合酶鏈反應方法,先以牛瘟之 RNA 製造 cDNA,供作後來的PCR增幅之用,此技術配合核酸定序技術即可檢測及區別牛瘟與小反芻獸瘟疫病毒。
| (A) |
樣品種類:
硬組織、週邊血液淋巴球 (PBLs)、眼睛或是嘴巴病變拭液。 |
| (B) |
引子種類:
| (a) |
樣品種類:
硬組織、週邊血液淋巴球 (PBLs)、眼睛或是嘴巴病變拭液。 |
| (b) |
引子核酸序列:
RP-1: 5'-GGCTCCCTGATTATGTTTCC-3'
RP-2: 5'-CTGGCGGTGCTGTTTGTTAT-3'
RP-3:5'-TCTCTCTGGGGGACTGATGC-3'(配合RP-2引子作為巢式引子) |
|
| |
|
| (C) |
RNA的萃取
| (a) |
依據Vangrysperre等 (1996) 之方法,以 TrizoI RNA reagent (Gibco) 萃取核酸。 |
| (b) |
硬組織 (0.5-1 g) 經剁碎,再以4 mL的細胞培養液將其均質化;眼睛或是嘴巴病變拭液製備成1mL;從5-10 mL全血純化的週邊血液淋巴球 (PBLs) 則泡製成0.4 mL。 |
| (c) |
上述樣品各取 0.2 mL,再加入 1 mL 之 TrizoI 試劑 (Gibco),震盪混合 30 秒,於室溫下靜置 5 分鐘,再加入 0.2mL 的氯仿 (chloroform),經震盪混合 30 秒後,於室溫靜置 3分鐘,再於 4℃ 以 12,000 g離心 15 分鐘,將其上層液與等量的異丙醇 (isopropanol) 充分混合後,於室溫下靜置 10分鐘,再以上述條件離心 10分鐘,倒除上層液之後,再加 0.05 mL 的 95% 酒精,以上述條件離心 5 分鐘,風乾,並溶解在 0.1 mL RNase free的滅菌水中,保存在-70 ℃或-20 ℃直到使用。 |
|
| |
|
| (D) |
反轉錄聚合酶鏈反應:
| (a) |
反應配方:
| dNTP (1.25mM) |
8 |
μL |
| 10x buffer (DNA polymerase) |
5 |
μL |
| primer (RP-1,RP-2) |
0.5 |
μL |
| rRNasin |
0.2 |
μL |
| AMV Rtase |
0.2 |
μL |
| DNA polymerase(2U/μL) |
0.5 |
μL |
| RNA template (1/12 RNA 萃取量) |
12.6 |
μL |
| DDW (Rnase free) |
23 |
μL |
反應總體積:50μL |
| (b) |
反應條件: |
| |
42℃ 40分鐘 → 95℃ 1分鐘
95℃ 30 秒 → 40℃ 60 秒→72℃ 60秒,共30個循環
72℃ 7分鐘 → 4℃ 保存 |
|
| |
|
| E. |
瓊脂膠片電泳分析:
| (a) |
瓊脂膠片製作: |
| |
秤取瓊脂膠 (agarose) 1.5g,加入 100 mL 的 1x TAE 電泳緩衝液,以微波爐加熱溶解瓊脂膠使成液態,置於 50 ℃ 恆溫水槽中,待溫度降至 50 ℃ 達平衡時,再加入 50 ng/ml 的溴化醯液 (ethidium bromide),使完全混合後,將膠液均勻倒入製膠臺中,再插上造孔板 (comb),待膠冷卻凝固後,小心拔出造孔板,並將膠片置入塑膠袋中,封緊後放入不透光紙袋內,再置入 4 ℃ 冰箱中保存。 |
| (b) |
RT-PCR產物載入 (loading) 膠片: |
| |
取一片膠,置入電泳槽中,槽中之電泳溶液須掩蓋過膠面,剪一片巴拉膠紙 (parafilm),撕開油紙面,將載入溶液 (loading dye) 滴在上面,使每滴為 1μL,滴的數目則比樣品數多一,再取樣品 10μL 與一滴載入溶液混合均勻後,即小心將混合液加入膠片的孔洞中,樣品均加完畢後,再取 DNA 標記與最後一滴的載入溶液混合,並加入孔洞。 |
| (c) |
電泳分析 |
| |
蓋上電泳槽之蓋子,將電極選定為"-"到"+",並選擇100 Volts 之按鈕,即可通電,約二十分鐘後,藍色條帶約跑到膠片上第四至五條線之間時,及可關掉電源。 |
| (d) |
UV 燈檢視 |
| |
將膠片自電泳槽中取出,置於 UV 燈檢視臺上,蓋上 UV 防護罩,開啟 UV 燈,即可檢視是否有預期大小之產物生成 (609 bp),若有則有可能是陽性反應,但必須經由依據同基因序列設計的巢式引子(RP-2與RP-3) 做進一步測試(產物大小為321 bp)或是將DNA產物進行核酸序列分析(為最佳選擇),才能作為進一步的確認。 |
| (e) |
在每一個RT-PCR反應中必須包括陽性對照,諸如痲疹或犬瘟熱病毒RNA及以滅菌水取代RNA的陰性對照。 |
|
|
|
|
| |
| 1. |
競爭性酵素結合免疫吸附法: |
| |
本法所需之試劑可向位於英國的O.I.E.牛瘟參考實驗室或是生物學診斷供應公司 (Biological Diagnostic Supplies Ltd; BDSL) 購得,其e-mail信箱為 mail@bdsl.uk.com。 |
| |
操作方法如下:
| (1) |
被覆抗原盤: |
| |
將冷凍乾燥的牛瘟抗原以1 mL的蒸餾水溶解,並以pH7.4的0.01 M磷酸緩衝生理食鹽水 (PBS) 稀釋成說明書上所建議的測試用濃度。立即分裝50μL的稀釋抗原至平底盤的適量孔洞中,在高度蛋白鍵結的ELISA微量盤(microplate),每個檢測血清用二個孔洞。輕輕敲打微量盤的邊緣,以確定抗原均完全的分佈在每個孔洞的底部,將盤子密封之後,再將其放入37℃定軌搖擺器上作用1小時。 |
| (2) |
製備阻斷緩衝液: |
| |
將Tween 20及正常牛血清加入0.01 M 磷酸緩衝液 (PBS) 中,使Tween 20 之終濃度成為0.1% (V/V),正常牛血清則為0.3%。
例如:製備100 mL之阻斷緩衝液時,則將0.1 mL之Tween 20及0.3 mL 之正常牛血清加入 100 mL 之磷酸緩衝液(PBS)中。 |
| (3) |
測試血清、對照血清及單株抗體的加入μL |
| |
在徹底以pH7.4的0.002 M PBS清洗每個孔洞三次之後(需避免盤子乾燥),分別加入40μL的阻斷緩衝液至每個血清檢測的孔洞中,隨後再加入10μL體積的所有測試及對照血清。並在單株抗體及結合體 (conjugate) 對照的孔洞中分別加入10μL及60μL的阻斷緩衝液,再依說明書上的建議,以阻斷緩衝液 (blocking buffer) 配製Mab的作用溶液,將此溶液50μL加入除了結合體(conjugate) 對照孔洞之其他孔洞中,清拍盤緣使反應液完全覆蓋孔洞之底部,再將盤子密封之後,再放入37℃溫室中的定軌搖擺器上搖擺作用1小時。將所有之血清及單株抗體放回 -20℃冰櫃中。 |
| (4) |
加入結合體 (conjugate): |
| |
在上述反應終了前,即依說明書上的建議,以阻斷緩衝液配製兔子抗老鼠免疫球蛋白馬-蘿蔔過氧化氫 (rabbit anti-mouse horse-radish peroxidase) 結合體的作用溶液,每盤需配6 mL,將保存之結合體 (conjugate) 先放回 -20℃冰櫃中。在反應終了時,徹底以pH7.4的0.002 M PBS清洗每個孔洞三次之後(需避免盤子乾燥),於每個測試的孔洞中加入此溶液50μL,清拍盤緣使反應液完全覆蓋孔洞之底部,再將盤子密封之後,放入37 ℃溫室中的定軌搖擺器上搖擺作用1小時。 (rabbit anti-mouse horse-radish peroxidase) 結合體的作用溶液,每盤需配6 mL,將保存之結合體 (conjugate) 先放回 -20℃冰櫃中。在反應終了時,徹底以pH7.4的0.002 M PBS清洗每個孔洞三次之後(需避免盤子乾燥),於每個測試的孔洞中加入此溶液50μL,清拍盤緣使反應液完全覆蓋孔洞之底部,再將盤子密封之後,放入37 ℃溫室中的定軌搖擺器上搖擺作用1小時。 |
| (5) |
加入受質/呈色質混合液及停止液: |
| |
在上述反應終了前,即將受質 (H2O2) 加入3.7 mM之呈色質 (OPD) 溶液中,使受質 (H2O2) 之終濃度為3.5 mM,此混合液是取24μL的H2O2加入6 mL之正-酚基二氨 (ortho-phenylene diamine; OPD) 溶液中。在上述反應終了時,徹底以pH7.4的0.002 M PBS清洗每個孔洞三次之後(需避免盤子乾燥),立即加入50μL體積的受質/呈色質混合液,置於室溫不需搖擺,作用10分鐘,每孔再加入由1M硫酸所組成的終止溶液 (stopping solution) 50μL。 |
| (6) |
此測試必須包括已知的牛瘟陽性及陰性血清樣品、Mab對照及結合體對照 (conjugate control)。 |
| (7) |
判讀: |
| |
以ELISA自動判讀機讀取樣品在492 nm波長的吸光值,測試結果與Mab對照所得的值比較後,以百分比抑制值來表示,抑制值達50%則為陽性,抑制值小於50%則為陰性。 |
|
| |
|
| 2. |
病毒中和作用試驗:
|
| |
實施中和試驗的方法如下:
| (1) |
試驗用種毒保存: |
| |
進行中和抗體測試之前先要準備一批試驗用疫苗株病毒種毒,先測試其病毒力價,再小分裝保存於 -80℃ 冰箱中,待每次進行中和試驗時取出稀釋使用。 |
| |
|
| (2) |
血清的處理: |
| |
將採集的血清經分裝保存於 -20℃,於血清測試前,須先經非動化的處理,方法是將已溶解回溫的血清放置在56 ℃水浴槽,靜置30分鐘後,以去除非特異反應因子,然後供為中和試驗用。 |
| |
|
| (3) |
實施方法:
| (A) |
稀釋血清: |
| |
先準備試管,做好記號後,分別加入 0.15 mL 細胞培養液做為血清的稀釋液,再取非動化 ( inactivated) 的血清 0.15 mL 加入第一管,而後依序連續以二倍稀釋至512倍,即完成稀釋。 |
| (B) |
病毒泡製: |
| |
取一支疫苗株病毒,待其溶解後,以細胞培養液做適當稀釋,使其成為每mL含有103.0 TCID50 的病毒。 |
| (C) |
細胞製備: |
| |
將小牛腎臟或VERO細胞自培養角瓶上,以trypsin消化下來,經沖散後,以細胞培養液泡成每mL含 2 x 105 個懸浮細胞,置於4℃中備用。 |
| (D) |
病毒與血清中和試驗: |
| |
於各個稀釋好的血清試管中,加入 0.15 mL 的103.0 TCID50 疫苗株病毒液,混合均勻後,置於4 ℃中過夜,之後再取其0.2 mL的體積,接種在滾軸管的每一管中,並立即加入1 mL懸浮在生長培養基的分散小牛腎臟或VERO細胞,其比例是每毫升含 2 x 105 個細胞,這些管子均斜放在37 ℃三天,之後那些出現病毒特異性的細胞病理學的管子則被拋棄;剩下管子中的培養基,改成維持培養液,然後反覆檢視至十天。 |
|
| |
|
| (4) |
結果判讀: |
| |
在血清的最後稀釋倍數是二倍若出現任何可檢測的抗體,則被認為是陽性。 |
| |
|
| (5) |
注意事項:
| (A) |
每個血清至少做2 管 (Duplicate)。 |
| (B) |
陽性、弱陽性、陰性血清之序列稀釋液亦需與試驗樣品一同操作,另加一組為未加稀釋血清做毒性對照。 |
| (C) |
每管加入0.2 mL 含有103.0 TCID50的疫苗株病毒液,在毒性對照則以培養液取代病毒液,細胞對照則是不加樣品血清不加病毒而加0.2 mL之培養液。 |
| (D) |
將殘餘的病毒原液以培養液做10倍序列稀釋至少4個梯度,每管使用0.2 mL,並且每稀釋倍數最少做4管供力價回歸測定。 |
| (E) |
若要計算終點 (end-points),病毒劑量則要落在每管101.8至102.8 TCID50之間。 |
| (F) |
微量盤的方法已被描述,其是用50μL的血清與50μL含101.8至102.8 TCID50的病毒稀釋液作用,在作用45分鐘或是過夜作用後,再加入 1 至 2 x 105 小牛腎臟、小羊腎臟或VERO細胞當作指示劑。此測試在6或7天後結束,本項檢測可以提供在高血清濃度時產生的非特異性中和作用的指標。 |
|
|
|
| |
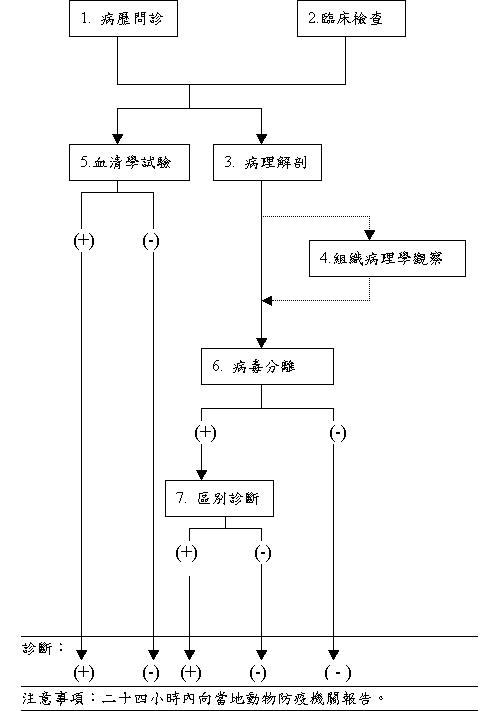
| 1. |
血清學試驗: |
| |
病材:配對血清 (paired sera)
方法:中和抗體力價測定 |
| |
|
| 2. |
病毒分離:
|
| |
病材:抗凝血分離白血球、脾臟腸繫膜淋巴結肩胛前淋巴結、糜爛期眼睛分泌物
方法:接種B95a小猿類淋巴胚細胞或初代小牛腎臟細胞或非洲綠猴腎臟(VERO)細胞 |
| |
|
| 3. |
病毒確認: |
| |
AGID或CIEP或反轉錄聚合酶鏈反應 |
|
 (rabbit anti-mouse horse-radish peroxidase) 結合體的作用溶液,每盤需配6 mL,將保存之結合體 (conjugate) 先放回 -20℃冰櫃中。在反應終了時,徹底以pH7.4的0.002 M PBS清洗每個孔洞三次之後(需避免盤子乾燥),於每個測試的孔洞中加入此溶液50μL,清拍盤緣使反應液完全覆蓋孔洞之底部,再將盤子密封之後,放入37 ℃溫室中的定軌搖擺器上搖擺作用1小時。
(rabbit anti-mouse horse-radish peroxidase) 結合體的作用溶液,每盤需配6 mL,將保存之結合體 (conjugate) 先放回 -20℃冰櫃中。在反應終了時,徹底以pH7.4的0.002 M PBS清洗每個孔洞三次之後(需避免盤子乾燥),於每個測試的孔洞中加入此溶液50μL,清拍盤緣使反應液完全覆蓋孔洞之底部,再將盤子密封之後,放入37 ℃溫室中的定軌搖擺器上搖擺作用1小時。