|
傳染性華氏囊病實驗室診斷標準操作程序(以下簡稱本標準)所制訂之內容係提供於實驗室處理相關病材,進行傳染性華氏囊病病毒分離鑑定及血清學試驗操作時參考之程序。 |
| |
| 1. |
傳染性華氏囊病(infectious bursal disease ,IBD): |
| |
傳染性華氏囊病亦稱甘保羅病(Gumboro disease),雖然雞、火雞、鴨、珠雞均可被感染,但只有雞感染會有臨床症狀,而且只有小雞會被感染。嚴重又急性的IBD通常引起高死亡率,但是一般較常見的是亞急性或無臨床症狀的IBD。由於病毒感染免疫器官華氏囊(bursa of Fabricius),故本病常造成二次感染的問題。 |
| |
|
| 2. |
傳染性華氏囊病病毒: |
| |
是一種雙股RNA病毒,被歸類於Birnaviridae。傳染性華氏囊病病毒會造成華氏囊之淋巴組織減損,如果此情形發生在2週齡之內的小雞,體液抗體(humoral antibody)反應就會被嚴重的抑制。目前傳染性華氏囊病病毒有兩種血清型,引起臨床疾病並且已有疫苗可使用的是IBD第一型。近來研究顯示有IBD第一型血清變異株發生,此需特別疫苗來做最大的保護,在許多國家IBD病毒非常強之毒株已經出現並且導致發生嚴重的病亦超過10年。 |
|
| |
本病可由特異的症狀與死後病變來作初步診斷。實驗室確診或無臨床症狀感染的偵測,可由體液免疫反應或組織內病毒抗原檢測來証明,若沒有這些試驗,華氏囊組織病理切片亦有所幫助。
| 1. |
材料與設備
| (1) |
37℃恆溫箱 |
| (2) |
孵蛋箱(恆溫35~37°C) |
| (3) |
照蛋器 |
| (4) |
打孔器 |
| (5) |
5000rpm離心機 |
| (6) |
超低溫冰櫃(-70~-100℃) |
| (7) |
倒立式光學顯微鏡 |
| (8) |
研缽 |
| (9) |
3-7週齡無特定病原雞與經IBD免疫過的雞 |
| (10) |
IBD抗體陰性之6至8日及9至11日齡雞胚胎 |
| (11) |
雞胚胎纖維芽細胞(CEF)培養於25cm2角瓶 |
| (12) |
螢光顯微鏡 |
| (13) |
吸管(1.2.5.10.20ml) |
| (14) |
1.c.c無菌注射針筒(針頭5/8×25G) |
| (15) |
10c.c無菌注射針筒(針頭18~20G×11/2) |
| (16) |
石臘或指甲油 |
| (17) |
70%酒精 |
| (18) |
碘酒棉花 |
| (19) |
14cm手術剪刀 |
| (20) |
-20℃冰箱 |
| (21) |
暗室 |
| (22) |
冷凍切片機 |
| (23) |
保濕盒 |
| (24) |
穿透式電子鏡 |
| (25) |
50000rpm 高速離心機 |
| (26) |
超微切片機 |
| (27) |
Grid |
| (28) |
粗濾紙 |
|
| |
|
| 2. |
試劑:
| (1) |
伊耳氏平衡鹽液(GIBCO) |
| (2) |
組織細胞培養液:每包 1 公升裝 MEM 鹽基粉末(GIBCO)加入滅菌再製蒸餾水至 1 公升。經溶解後加入 2.3 gm 的 NaHCO3,以 0.22μ Millipore 過濾並分裝於 500 mL 血清瓶內,TSA Agar無菌檢定通過後放入 4 ℃ 冰箱備用。 |
| (3) |
病材乳劑緩衝液:PBS中添加penicillin (10,000iu/ml),streptomycin (1,000μg/ml)及0.5% (W/V)牛白蛋白,最後調整pH7.2,0.45μm濾膜過濾,保存於4℃ |
| (4) |
中性福馬林(Fisher) |
| (5) |
IBDV抗血清 |
| (6) |
甲醇(Merck) |
| (7) |
冰冷丙酮:丙酮(Merck)放置於-20℃冰箱 |
| (8) |
IBDV-FITC螢光標示抗體 |
| (9) |
PBS:
| NaCl |
(Merck) |
8.0 |
gm |
| KCl |
(Merck) |
0.2 |
gm |
| Na2HPO4.7H2O |
(Merck) |
2.17 |
gm |
| KH2PO4 |
(Merck) |
0.2 |
gm |
| 加蒸餾水至 |
|
1,000 |
mL |
以121 ℃ 15 磅 / cm2高壓滅菌20分鐘。 |
| (10) |
電顯用固定液:2﹪formaldehyde |
| (11) |
電顯負染色液: Phosphotungstic acid (24 WO3.2H3PO4.48H2O) |
|
| |
|
| 3. |
病毒分離:
| (1) |
病材準備:
| (a) |
以無菌操作摘取5個早期感染之華氏囊,將它切碎。 |
| (b) |
加入少量含有抗生素(penicillin 1000 unit/ml與streptomycin 1,000μg/ml)及0.5%(W/V)牛白蛋白之磷酸緩衝液(PBS, pH7.2 ),以研缽將其磨碎均質化,做成10倍乳劑,保存於-20℃。 |
| (c) |
使用前將此均質液以3,000g離心10分鐘,回收上清液,用做後續的檢驗。 |
|
| |
|
| (2) |
細胞培養分離法:
傳染性華氏囊病病毒可培養於華氏囊細胞(BF)及雞胚胎腎細胞(CEK)或雞胚胎纖維芽細胞(CEF),但培養之前兩代可能無細胞病變效應(CPE)產生,可用免疫螢光染色法來鑑定,免疫螢光染色法於接種後48小時進行之。
| (a) |
取4支長滿無特定病原雞(SPF)來源之雞胚胎纖維芽細胞(CEF) 25cm2組織培養瓶,各接種0.5ml樣品,在37℃吸附30分鐘。 |
| (b) |
以伊耳氏平衡鹽液洗2次。 |
| (c) |
加入細胞維持液,放37℃恆溫箱培養。 |
| (d) |
每日於倒立式光學顯微鏡下觀察是否有細胞病變效應(cytopathic effect ,CPE),若有則會有圓形折射性細胞出現。 |
| (e) |
觀察6天後仍沒有CPE,則將它冷凍解凍後溶液接種新的細胞,此步驟可能需要重複至少3次。 |
| (f) |
若發現CPE,則病毒應以IBD血清進行中和試驗 (virus neutralization ,VN) 鑑定病毒。 |
|
| |
|
| (3) |
雞胚胎分離法:
本法為IBDV例行性分離診斷最常使用之方法,但需連續繼代則較費時。
| (a) |
取5個IBD抗體陰性之6至8日齡雞胚胎,接種0.2ml樣品入卵黃囊。 |
| (b) |
同時取5個IBD抗體陰性之9至11日齡雞胚胎,接種0.2ml樣品入絨毛漿尿膜上。 |
| (c) |
每日照蛋,48小時以內死亡者丟棄,胚胎在接種後2日至7日死亡者收集雞胚胎及絨毛漿尿膜,第7日以後雞胚仍活存之雞胚乳劑繼續繼代,最多繼5代來檢查病變。 |
| (d) |
胚胎通常於接種後3至6日死亡。IBD可造成胚胎矮化、皮下水腫、充出血。肝臟腫大,呈斑點狀出血。若死亡較晚者則肝臟呈綠色腫大,並有壞死。腎腫大且斑狀充血、脾亦腫大。 |
|
| |
|
| (4) |
雞隻分離法:此方法分離IBD病毒最簡單。
| (a) |
取5隻有感受性的雞與5隻經IBD免疫過的雞(3-7週齡), 以點眼、口服、點肛或肌肉注射方式,每隻雞接種0.05ml樣品,其中以點眼方式接種最常使用。 |
| (b) |
接種後72-80小時,剖檢華氏囊,檢查華氏囊病變;病毒感染的華氏囊呈黃色(有時出血)腫大,有明顯的細溝,華氏囊周邊水腫亦常見,華氏囊內有時可見乳酪化物質,華氏囊褶襞有出血點。 |
| (c) |
若有感受的雞呈現此病變,同時免疫過的雞沒有病變則可診斷為IBD。 |
| (d) |
另一方法為取3-5週齡無IBD抗體雞隻10隻,以點眼、口服、點肛或肌肉注射方式,每隻雞接種0.025ml樣品,接種後第0、3、5、7日各檢查2隻雞之華氏囊肉眼病變及組織學病變,取下之華氏囊一部份放中性福馬林重做組織病理檢查用,另一部份保存於-20℃冷凍。 |
| (e) |
上法判定華氏囊病變,若無病變者表示非IBD。 |
| (f) |
病毒鑑定:將產生華氏囊病變結果之病材用已知IBD陽性抗血清處理中和後,再接種雞胚胎或雞隻鑑定是否為IBDV。 |
| (g) |
組織染色可在CPE附近的細胞核內看到Cowdry's type A的核內包涵體,以及多核巨大細胞 (polykaryocyte)。 |
|
|
| |
|
| 4. |
病毒鑑定:
| (1) |
免疫螢光法(IF):
| (a) |
試材:組織培養細胞接種病材產生CPE時,棄培養液以甲醇固定組織10分鐘,或病材接種隻雞隻華氏囊病材以冷凍切片機切片及以冰冷丙酮固定。 |
| (b) |
染色步驟;將標示FITC螢光抗體適倍量稀釋(通常稀釋1000倍)滴於此已固定之待測培養細胞上。 |
| (c) |
置於保濕盒,密封蓋緊,放37℃感作1小時後,取出以PBS緩衝溶液浸洗三次,每次五分鐘。 |
| (d) |
在螢光顯微鏡下觀察,特異蘋果綠色螢光可在感染細胞的細胞質出現。 |
|
| |
|
| (2) |
凝膠免疫擴散法(AGP):
| (a) |
檢測華氏囊內抗原:取10隻急性感染期之華氏囊,切碎研磨後,置於AGID盤內孔洞中以陽性血清檢測。 |
| (b) |
試驗步驟如血清學試驗四-4。 |
|
| |
|
| (3) |
電子顯微鏡觀察:
| (a) |
將華氏囊病材或經接種之雞胚胎做成乳劑或接種細胞液,先以10000-11500rpm 高速離心取上清。 |
| (b) |
再以30000-35000rpm 離心2小時,取沉澱物。 |
| (c) |
將沉澱物懸浮於小量的蒸餾水中,取一滴於玻片上,加上一滴Phosphotungstic acid (24 WO3.2H3PO4.48H2O)染色。 |
| (d) |
混合後滴在Grid上,以剪成尖角狀之粗濾紙以毛細現象吸掉多餘液體。 |
| (e) |
放入穿透式電子鏡檢查。 |
| (f) |
或將上述病材先以2﹪formaldehyde在4℃固定至少2小時,製作超微切片,以電子顯微鏡觀察。 |
| (g) |
病毒顆粒70nm大小,無封套,正20面體。 |
|
|
|
| |
本病在一群雞中通常散佈快速。因此只需要測定一小部份雞血清即可。未免疫雞隻若是發現陽性反應,就視為整群雞均被感染。
| 1. |
材料與設備
| (1) |
5000rpm離心機 |
| (2) |
熱水槽(50-100℃) |
| (3) |
均質機 |
| (4) |
-40℃冷凍庫 |
| (5) |
-20℃冰箱 |
| (6) |
37℃ 5﹪CO2恆溫箱 |
| (7) |
3-5週齡SPF小雞 |
| (8) |
9cm塑膠平皿(Petri dish)或25×75mm之載玻片 |
| (9) |
天秤 |
| (10) |
保鮮盒 |
| (11) |
無菌96孔平底組織培養微量盤 |
| (12) |
計時器 |
| (13) |
ELISA reader (Titertek Multiscan) |
| (14) |
20-200μl八爪微量分注器(Coster) |
| (15) |
研缽 |
| (16) |
暗室 |
| (17) |
透明膠帶(8-12cm 寬) |
| (18) |
4℃冰箱 |
|
| |
|
| 2. |
試劑:
| (1) |
Methylene chloride蒸餾水 |
| (2) |
磷酸緩衝溶液 (phosphate buffered isotonic saline , PBS , pH 7.0-7.4):
| NaCl |
(Merck) |
8.0 |
gm |
| KCl |
(Merck) |
0.2 |
gm |
| Na2HPO4.7H2O |
(Merck) |
2.17 |
gm |
| KH2PO4 |
(Merck) |
0.2 |
gm |
| 加蒸餾水至 |
|
1,000 |
mL |
以121 ℃ 15 磅 / cm2高壓滅菌20分鐘。並以T.S.A. Agar 作無菌檢定。 |
| (3) |
病毒中和試驗相關試劑:
| (a) |
M199組織培養液:medium199(GIBCO)中加
10﹪tryptose phosphate broth
1.5﹪的5.6﹪碳酸鈉溶液
0.5﹪的0.3M Hepes solution
penicillin 100μg/ml
streptomycin 100μg/ml
fungizone 2.5μg/ml
使用時另加l2﹪fetal calf serum(經熱非動化過) |
| (b) |
IBD病毒液:IBDV-GT101(或IBD其他標準病毒株),以M199組織培養液稀釋成每25μl含100 TCID50(50﹪組織培養感染劑量)的病毒液 |
| (c) |
CEF細胞懸浮液:將10日齡雞胚胎去頭去四肢後以Trypsin消化組織製成之單一或小細胞團懸浮液,細胞用M199組織培養液洗一次並懸浮成75x104細胞/ml |
| (d) |
1﹪Crystal violet溶液:95﹪酒精100ml加1gmCrystal violet (1﹪) |
|
| (4) |
凝膠:
| 氯化鈉(NaCl) |
80 |
克 |
| 石碳酸(phenol) |
5 |
克 溶於1升之蒸餾水,加凝膠(Noble agar) 12.5克 |
煮沸直至完全溶解,20ml小分裝至玻璃內,4℃保存備用。 |
| (5) |
酵素連結免疫分析(ELISA)相關試劑:
| (a) |
IgG兔抗IBDV高免血清:兔子之IgG以blue dextran (Pharmacia) 或protein A (Pharmacia)色層分析管柱純化獲得。 |
| (b) |
0.05M Carbonate- bicarbonate buffer (pH9.6) |
| (c) |
0.05﹪Tween 20之PBS (PBST) |
| (d) |
5﹪脫脂奶粉 |
| (e) |
綿羊抗雞Ig Conjugated horseradish peroxidase (KPL) |
| (f) |
Recrystallised 5- aminosalicyclic acid (Merck) |
| (g) |
0.1M hydrogen peroxide (H2O2) |
|
|
| |
|
| 3. |
病毒中和試驗
| (1) |
試驗步驟
| (a) |
病毒稀釋成每0.05ml含有100 TCID50分裝入96孔組織培養盤,每孔0.05ml。 |
| (b) |
待測血清先以56℃ 30分鐘非動化後,在分裝好病毒的96孔盤中2倍連續稀釋血清,37℃ 感作1小時。 |
| (c) |
感作後每孔加入0.2ml雞胚胎纖維芽細胞懸浮液(CEF)後,置於37℃ 5﹪CO2恆溫箱培養4至5天。 |
| (d) |
去除盤內各孔之培養液,加入0.05ml 1﹪結晶紫染色液染色1分鐘。 |
| (e) |
用水緩和洗數次,最後使其乾燥。 |
|
| |
|
| (2) |
判讀:
| (a) |
當細胞存在時,結晶紫染劑染在細胞上會呈現暗紫色,當細胞死亡脫落,只有輕微染色或無色。 |
| (b) |
判讀每個血清列最後暗紫色孔的血清稀釋倍數,血清完全被病毒中和之稀釋倍數的倒數是為血清力價。 |
|
| |
|
| (3) |
對照:
| (a) |
陽性及陰性對照 |
| (b) |
病毒對照:病毒原液稀釋成10-2至10-9做四重複,以確定試驗中加入的病毒量對否。 |
| (c) |
血清對照:初步稀釋的血清與CEF感作,不加病毒,檢測血清對細胞的毒性作用。 |
|
|
| |
|
| 4. |
凝膠免疫擴散試驗
| (1) |
檢測血清樣品:採取感染早期及感染3週後之血清樣品各20個。 |
| (2) |
檢測華氏囊內抗原:取10隻急性感染期之華氏囊,切碎研磨後,置於AGID盤內孔洞中以陽性血清檢測。 |
| (3) |
陽性對照抗原之準備:
| (a) |
取IBD病毒感染之華氏囊加磷酸緩衝液,研磨成10%均質液 |
| (b) |
離心3000g 10分鐘,取上清液 |
| (c) |
上清液點眼接種3-5週齡有感受性之小雞。 |
| (d) |
接種後3天無菌摘取華氏囊,出血的華氏囊丟棄,其它集合後稱重 |
| (e) |
加入等量之冷蒸餾水,再加一份等量之Methylene chloride,在均質機打碎混合後,以2,000g離心30分鐘,取上清液小分裝後-40℃冷凍保存。 |
|
| (4) |
陽性對照抗血清之準備
| (a) |
將IBD病毒感染之華氏囊做成10%均質液,離心3000g 10分鐘 |
| (b) |
取上清液點眼接種4-5週齡SPF小雞,每隻接0.05ml |
| (c) |
接種後28天採血,將血清小分裝置於-20℃保存。 |
|
| (5) |
試驗步驟
| (a) |
試驗前24小時至7天準備平板,將凝膠置於沸水浴溶解。 |
| (b) |
將9cm塑膠平皿 (Petri dish) 置於水平桌面,1瓶凝膠20ml,倒入一膠質平板(或將凝膠加在25×75mm之載玻片上,打直徑3mm孔,孔距6mm)。 |
| (c) |
將平皿蓋上蓋子,凝膠凝固後保存於4℃備用。此可儲存7天(如果凝膠平皿當天就要使用,可將平皿打開倒置於37℃溫箱乾燥30分鐘至1小時即可使用)。 |
| (d) |
用圓柱狀切割器切割出三排垂直的孔。 |
| (e) |
切出的凝膠,從孔中去除,必需注意不可將孔壁破壞。 |
| (f) |
加待測血清至孔中9分滿,或加華氏囊乳劑待測抗原到孔中9分滿。 |
| (g) |
加陽性與陰性對照入相關孔中。每一待測血清或華氏囊乳劑均應排列在陽性抗體與抗原之旁邊。 |
| (h) |
將平皿置於22℃至37℃之保鮮盒中感作48小時。 |
| (i) |
將平皿置於暗背景與斜光源之上觀察判讀沉降線。 |
|
|
| |
|
| 5. |
酵素連結免疫分析(ELISA):本法用於檢測感染組織內IBDV
| (1) |
試驗步驟:
| (a) |
在室溫中以平底96孔塑膠微量盤進行,盤底包覆100μl IgG兔抗IBDV高免血清,兔抗IBDV高免血清先以0.05M Carbonate- bicarbonate buffer (pH9.6) 稀釋。 |
| (b) |
包覆後之盤子用透明寬膠帶封緊,放置室溫隔夜。 |
| (c) |
盤子用含0.05﹪Tween 20之PBS (PBST)洗3次,洗液停置盤內至少1分鐘。 |
| (d) |
IBD抗原用過濾過之洗液加5﹪脫脂奶粉稀釋(稀釋液)後,每孔加100μl。 |
| (e) |
盤子感作1小時後,以洗液洗3次。 |
| (f) |
抗血清以稀釋液倍比連續稀釋,加100μl至盤內。 |
| (g) |
盤子再感作1小時,以洗液洗3次。 |
| (h) |
綿羊抗雞Ig Conjugated horseradish peroxidase (KPL) 以稀釋液稀釋1:1000後,每孔加100μl。 |
| (i) |
感作1小時後,以洗液洗3次,最後一次用蒸餾水洗。 |
| (j) |
Recrystallised 5- aminosalicyclic acid (Merck) 加入預先泡好的0.1M hydrogen peroxide (H2O2) 0.2 ml,再加入盤子每孔100μl。 |
| (k) |
放震盪器上震盪30分鐘後,在450nm波長ELISA reader (Titertek Multiscan)判讀OD值。 |
|
| |
|
| (2) |
ELISA試劑稀釋濃度及對照設定:
| (a) |
以上所使用的每批包覆抗體、IBDV抗原及抗雞Ig conjugate等試劑皆須先測定其最適當使用濃度,在背景值為最小的情況下,其OD值最大在1.10- 1.20之間。 |
| (b) |
陰性血清或低濃度抗體血清通常稀釋1:200,結合背景值時ELISA終點取0.15 OD。 |
| (c) |
對照孔需無抗原但有包被抗體、雞血清及Conjugate。 |
| (d) |
只有雞血清的孔可以省略掉,而以只有稀釋液的孔取代之。 |
| (e) |
每列剩下來除了有加過Substrate者以外,其他未經處理的孔可以作為reader的'Blanked'。 |
| (f) |
ELISA法檢測抗體與中和試驗法檢抗體一樣敏感,兩種方法之敏感性皆大於凝膠免疫擴散法100倍。 |
|
|
|
| |
|
| 1. |
動物傳染病診斷標準。雲林縣家畜疾病防治所彙編。 |
| 2. |
禽病檢查手冊。宋華聰、林茂勇編校。藝軒圖書出版社。1995。 |
| 3. |
Manual of Standards for Diagnostic Tests and Vaccines. Office International des Epizooties, World Organisation for Animal Health. 1997. |
|
| |
| 1. |
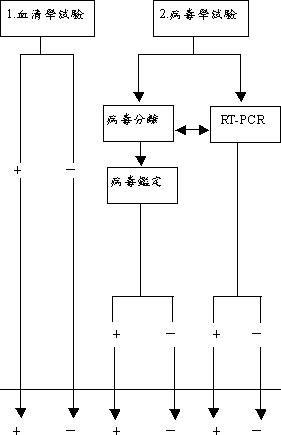
血清學試驗 |
| |
方法:病毒中和試驗(VN)、ELISA或AGP抗體抗體呈現陽性。 |
| |
|
| 2. |
病毒學試驗
|
| |
方法:接種於10-12日齡雞胚胎、已形成單層細胞之BHK-21、VERO細胞等株化細胞。
| A. |
RT-PCR陽性檢體需進行定序 |
| B. |
病毒分離:雞隻接種分離法、雞胚胎分離法、雞胚胎纖維芽細胞(CEF)培養分離法。 |
| C. |
病毒鑑定:IF、TEM、RT-PCR。 |
|
|