|
馬立克病實驗室診斷標準操作程序(以下簡稱本標準)所制訂之內容係提供於實驗室處理相關病材,進行馬立克病病毒分離鑑定及血清學試驗操作時參考之程序。 |
| |
| 1. |
馬立克病(Marek's disease, MD):為一種雞的淋巴腫瘤及致神經病變疾病,其病原為泡疹病毒(Herpesvirus)。 |
| 2. |
淋巴腫瘤:淋巴細胞呈不正常增生。 |
| 3. |
神經麻痺:感染馬立克病病雞腿部及翼部的神經局部或完全痲痹。 |
| 4. |
細胞附存性(cell associated):病毒存在於感染細胞內,不釋放到細胞外。 |
| 5. |
白血球層(buffy coat):血液離心後介於紅血球層與血漿之間的白色薄層。 |
| 6. |
毛囊尖端(follicular tip):在皮膚內之羽軸部分。 |
| 7. |
多核巨大細胞 (polykaryocyte):病毒感染後數個細胞融合一起成一個多細胞核的大細胞。 |
| 8. |
HVT:火雞泡疹病毒,對雞隻無病原性,但可產生交叉免疫抗體,因此多用於當雞隻馬立克病疫苗。 |
|
| |
典型的馬立克病最常見的臨床病徵為腿部及翼部的局部或完全痲痹。而在急性型,感染病禽通常可見極度抑鬱及甚至並無出現任何症狀即死亡。
| 1. |
典型的MD:
| (1) |
典型的MD中具特徵性的發現為一至數條周圍神經(peripheral nerve)的腫大。這些通常在死後剖檢時最容易見於翼神經叢、坐骨神經叢、腹腔神經叢、腹腔迷走神經及肋間神經等。變性的神經通常腫至正常的2-3倍大,正常時所見的橫斷面橫紋及閃亮光澤消失,外觀可能呈現淡灰或淡黃色﹐有時甚至水腫。 |
| (2) |
淋巴瘤有時見於典型的馬立克病,以卵巢中形成質軟灰色的小腫瘤最常見,但有時在肺、腎、心、肝及其他組織亦可發現。 |
|
| |
|
| 2. |
急性型的MD:
| (1) |
具特徵性的病變為迷漫性淋巴瘤的轉移,涉及臟器包括有肝、性腺、脾臟、腎、肺、前胃及心。有時淋巴瘤也在骨骼肌或羽毛濾泡周圍附近的皮膚發生。 |
| (2) |
染的病禽有如同典型病型的神經腫大。 |
| (3) |
於年輕病禽其肝臟呈中度腫大,而成年病禽的肝臟則如同淋巴白血病所見呈較大腫大。但神經的傷害往往不見於成年病禽。 |
|
| |
|
| 3. |
綜合病變:
| (1) |
急性型及典型MD中﹐疾病發生始於淋巴細胞的增生,增生的形式可能在某些為發展性增生而在其他則為退型性增生。 |
| (2) |
周邊神經所受的影響可能為增生性(proliferative)、炎症性(inflammatory)、中度浸潤性(minor infiltration)的變化而分成為A型、B型及C型病灶。 |
| (3) |
A型造成的病灶包括有增生性淋巴母細胞、大中小型淋巴球、巨噬細胞的浸潤,特性上均為增生性的。 |
| (4) |
B型造成的病灶則以特徵性的神經內水腫、小型淋巴球及漿細胞的浸潤、許旺氏細胞的增生;特性上屬炎症性反應。 |
| (5) |
C型病灶包括有常見於無大體病變及臨床症狀的病禽可見到的小型淋巴球散佈。這種病灶被認為是進展性的發炎反應。 |
| (6) |
而脫髓鞘通常發於A型及B型,並造成臨床上所見的痲痹。 |
| (7) |
於內臟器官或其他組織所見的淋巴瘤和A型於神經所造成的淋巴增生在細胞形態上是類似的。 |
| (8) |
通常這些淋巴細胞增生都是混合多樣的,其中又以小中型淋巴細胞為最多;有時,特別是在成年急性的病例中可見多數的大型淋巴細胞及淋巴母細胞。 |
| (9) |
這種在淋巴瘤所見的異源性(heterogenous)淋巴細胞族群,可用蘇木紫伊紅(haematoxylin eosin)染色及淋巴瘤壓片May-Grunwald-Giemsa染色並可與淋巴白血病加以區別,因淋巴白血病所見的為單純(uniform) 淋巴母細胞的浸潤。 |
| (10) |
另外一個重要的區別為於淋巴白血病中,淋巴瘤發生於華氏囊且為內濾泡源生性並有增生的情形。 |
| (11) |
在MD雖然有時華氏囊亦有淋巴增生發生、但腫瘤在所在位置處較不明顯、呈擴散及濾泡間增生性等。 |
| (12) |
周邊神經的傷害在淋巴白血病中並不如MD般為病變的特色。 |
| (13) |
區別成年禽類的MD與淋巴白血病時最大的困難在於MD有時有淋巴增生性腫瘤伴隨肝臟腫大而無神經病變的情形發生。 |
|
|
| |
根據臨床病症、大體及顯微病變加以診斷此病。雞隻感染馬立克病病毒並不一定呈現臨床症狀,但病毒感染可利用病毒分離或病毒抗原與抗體的反應來加以偵測。MD病毒有兩種血清型被加以確認,分別為1及2型,第3型血清型則為火雞泡疹病毒(HVT)。
| 1. |
材料與設備
| (1) |
38.5℃ CO2恆溫箱 |
| (2) |
5000rpm離心機 |
| (3) |
超低溫冰櫃(-70~-100℃) |
| (4) |
液態氮保存桶 |
| (5) |
超音波擊碎器 |
| (6) |
倒立式光學顯微鏡 |
| (7) |
雞腎細胞或鴨胚纖維芽細胞培養用設備 |
| (8) |
0.45μ過濾膜 |
| (9) |
吸管(1.2.5.10.20ml) |
| (10) |
60mm直徑塑膠細胞培養皿 |
| (11) |
研缽 |
| (12) |
4日齡雞胚蛋(本所檢定分所生產) |
| (13) |
9-11日齡雞胚蛋(本所檢定分所生產) |
| (14) |
1ml、5ml、10ml注射針筒 |
| (15) |
照蛋器 |
| (16) |
37℃恆溫箱 |
| (17) |
含抗凝血劑(肝素)試管 |
| (18) |
一日齡SPF小雞 |
| (19) |
正壓或負壓Horsfall-Bauer 隔離箱 |
| (20) |
15cm有鉤鑷子及手術剪刀 |
| (21) |
細胞消化瓶(含磁鐵) |
| (22) |
組織切片機及組織染色組 |
|
| |
|
| 2. |
試劑:
| (1) |
SPGA-EDTA(sucrose, phosphate, glutamate and albumin-ethylene diamine tetra-acetic acid)緩衝液:
0.2180M sucrose(7.462g)
0.0038M monopotassium phosphate(0.052g)
0.0072M dipotassium phosphate(0.125g)
0.0049M L-monosodium glutamate(0.083g)
1.0% bovine albumin powder(1.000g)
0.2% EDTA(0.200g)
distilled water(100ml)
以0.45μm濾膜過濾並將pH值調至6.5 |
| (2) |
組織細胞培養液 (商品化Eagle's minium essential medium)(GIBCO) |
| (3) |
PBS 緩衝液 |
| (4) |
0.25% Trypsi
Trypsin 250 g溶於1000 ml PBS中,以0.45μm 過濾膜過濾 |
| (5) |
細胞液態氮保存液:MEM 75%,DMSO 10%,胎牛血清 15% |
| (6) |
雞腎細胞或鴨胚纖維芽單層細胞 |
| (7) |
中性福馬林 |
| (8) |
甲醇 |
| (9) |
MDV陽性抗血清 |
| (10) |
鹽類瓊膠:8﹪Sodium chloride 加0.7﹪Difco bactoagar |
| (11) |
抗雞免疫球蛋白螢光標示抗體 |
|
| |
|
| 3. |
病毒分離:
| (1) |
檢體:因MD細胞為強烈細胞附存性(cell associated)故這類細胞懸浮液必須要含有活存細胞。
A、白血球層(buffy coat):
| (a) |
自感染四週齡左右之毒血症病雞採取。 |
| (b) |
抽取之血液加入含肝素的抗凝血試管中,血液樣本離心1,000rpm 10分鐘,取白血球層(buffy coat)細胞懸浮於MEM。 |
B、腫瘤組織臟器:淋巴瘤細胞懸浮液或脾臟細胞懸浮液
| (a) |
以無菌操作採取感染雞之脾或腎等內臟腫瘤 |
| (b) |
以PBS緩衝液清洗除去血球 |
| (c) |
剪碎臟器並以胰蛋白脢(0.25% trypsin)消化成小團細胞作為接種病材。 |
| (d) |
非馬上接種之材料則懸浮於細胞液態氮保存液內分裝保存。 |
C、毛囊尖端(follicular tip):無細胞依附之馬立克病病毒可自此地方加以萃取分離
| (a) |
拔取病雞羽毛,取毛囊5mm的尖端或絞碎含尖端通到皮膚的樣本,置入研缽內剪碎研磨 |
| (b) |
以SPGA-EDTA緩衝液做成5至10倍乳劑。 |
| (c) |
以超音波擊碎器處理2分鐘,再以650xg離心10分鐘,上清液以0.45μ過濾膜加以過濾。 |
|
| |
|
| (2) |
細胞培養分離法:
| (a) |
將檢體細胞懸浮液0.2ml (含106-107活細胞) 接種至60mm直徑塑膠細胞培養皿培養24小時之單層雞腎細胞(CK)或鴨胚纖維芽細胞(DEF)內,置於38.5℃,5 % CO2恆溫箱中進行培養。 |
| (b) |
培養24小時後,更換培養液。 |
| (c) |
每日在倒立光學顯微鏡下觀察細胞病變效應(CPE),並依培養液酸鹼顏色變化約每3天更換一次培養液。 |
| (d) |
大約在接種後3-5天出現圓形化細胞病變效應(CPE)。 |
| (e) |
組織染色可在CPE附近的細胞核內看到Cowdry's type A的核內包涵體,以及多核巨大細胞(polykaryocyte)。 |
|
| |
|
| (3) |
毛囊尖端(follicular tip)分離法:
| (a) |
毛囊病材處理後接種至培養24小時的單層雞腎細胞(CK),38.5℃恆溫箱感作40分鐘。 |
| (b) |
加入培養液後置於38.5℃,5 % CO2恆溫箱中進行培養7天,每日觀察CPE。 |
|
| |
|
| 4) |
小雞接種分離法:本法常用於病毒株之繼代保存。
| (a) |
病材接種於一日齡小雞腹腔內。 |
| (b) |
接種小雞飼養於具有空氣過濾的正壓或負壓式 Horsfall - Bauer隔離箱,以防試驗雞感染外界病毒。 |
| (c) |
接種後6-8週,解剖檢查肉眼病變及將試驗雞隻內臟取下放中性福馬林中,以便製作組織切片觀察顯微鏡下馬之克病之病變,同時採集試驗雞血清作下列血清學檢查證明病毒感染。 |
|
| |
|
| (5) |
雞胚接種法:
本法用以接種後雞胚絨毛尿囊膜(CAM)產生痘泡 ( Pock) 來判定,連續繼代以適應於細胞培養的MDV,在雞胚CAM上產生痘泡的能力會減低。
| (a) |
初代分離用病材白血球層或腫瘤組織臟器接種於4日齡雞胚卵黃囊中,或以靜脈注射法注入10-11日齡雞胚血管。 |
| (b) |
病材毛囊尖端(游離病毒)則接種於9-12日齡雞胚之CAM |
| (c) |
分接種組與對照組,培養於37℃恆溫箱,每日照蛋檢查。 |
| (d) |
接種後24小時以內死亡者丟棄。以後死亡者之雞胚檢查CAM有無痘泡 |
| (e) |
無死亡雞胚觀察至18日齡。 |
| (f) |
雞胚CAM上有Pock者判定病毒陽性。 |
|
|
| |
|
| 4. |
病毒鑑定:
| (1) |
同居感染試驗:
| (a) |
前述一日齡小雞接種病材後,在病材接種小雞之隔離箱內同時放一些無接種雞,飼養於隔離箱6-8週 |
| (b) |
檢查其試驗雞及同居感染雞之肉眼或顯微病變。 |
| (c) |
若病材內只存在HVT (火雞泡疹病毒)接種雞不會水平傳播HVT,而MDV之病材接種雞則會空氣傳播給同居感染雞 |
|
| (2) |
血清型別病毒斑之判讀:紀錄病毒斑(plaque)形成的時間及形態學特徵,據以分辨不同血清型別的病毒所造成的病毒斑(HVT形成的病毒斑出現較早且比血清1型大,而血清2型病毒斑則比血清1型較晚出現且較小。) |
| (3) |
免疫螢光法(IF):
| (a) |
組織培養細胞接種MDV,經37℃培養4天左右產生CPE時,棄培養液以甲醇固定組織10分鐘(此經固定之組織培養抗原沒有使用時可保存於-70℃備用)。 |
| (b) |
染色步驟;將標準MDV陽性血清滴於此已固定之待測培養細胞上。 |
| (c) |
置於保濕盒,密封蓋緊,放37℃感作1小時後,取出以PBS緩衝溶液浸洗三次,每次五分鐘。 |
| (d) |
滴上適當稀釋倍數(通常稀釋1000倍)之標示螢光第二抗體(抗雞球蛋白螢光標示抗體),如前述步驟,置於保濕盒在37℃作用30-60分鐘後,取出再以PBS浸洗三次。 |
| (e) |
在螢光顯微鏡下觀察,特異蘋果綠色螢光可在感染細胞的細胞核和細胞質出現。 |
|
| (4) |
羽毛尖端檢測病毒膠內免疫擴散法:
A、試劑:
馬立克抗血清凝膠:以8% sodium chloride 溶液加0.7% Difco bactoagar ,沸騰溶解後將溫度下降維持至47℃,添加馬立克病病毒抗血清混合均勻,分裝覆於載玻片上。
B、步驟:
| (a) |
待檢雞隻的小羽毛尖端樣本垂直插入凝膠內,將載玻片置放在潮溼培養皿,37℃下作用24小時後,在暗室利用燈光進行結果判讀。 |
| (b) |
若在羽毛尖周圍出現放射狀沈澱線表示羽毛內含有MD病毒抗原﹐亦表示感染發生。 |
|
|
|
| |
|
4週齡以後雞隻如發現有MD的抗體表示有感染發生。4週齡以前抗體出現表示可能來自卵黃囊的母體移行抗體而並不能當成主動感染的證據。抗MD的抗體通常在感染1-2週後產生,抗體的偵測及確認一般以膠內免疫擴散(agar gel immunodiffusion)進行反應,有時亦以其他血清學方法來進行偵測。病毒、抗原及抗體可自OIE的馬立克病參考實驗室取得。
| 1. |
材料與設備
| (1) |
熱水槽 |
| (2) |
均質機 |
| (3) |
吸管(10 ml) |
| (4) |
液態氮桶 |
| (5) |
37℃恆溫箱 |
| (6) |
2000rpm 離心機 |
| (7) |
AGID反應試驗材料及設備:25×75mm載玻片、吸引針、鑿孔器、暗室、判讀箱 |
| (8) |
ELISA反應試驗材料及設備:96孔盤離心機、ELISA reader(Titertek Multiscan)、平底96孔塑膠微量盤 |
|
| 2. |
試劑
| (1) |
MD標準陽性抗原:分讓自OIE參考實驗室或刮取感染MDV產生CPE的細胞以超音波處理後,650xg離心10分鐘之上清液或羽毛尖端的萃取物。 |
| (2) |
MD標準陽性抗血清: 分讓自OIE參考實驗室或自行免疫 |
| (3) |
CEF或DEF細胞 |
| (4) |
組織液態氮保存液:係於每 100 mL MEM 細胞培養液內加入 10 mL 胎牛血清(10%)及10 mLDMSO (10%),供組織細胞液態氮保存用 |
| (5) |
細胞消化液:100 ml PBS溶液中加入0.25g Trypsin(Sigma),於4℃磁性攪拌溶解後,0.45μm過濾膜過濾 |
| (6) |
AGID反應用凝膠:8%氯化鈉 (NaCl) 溶液加0.7﹪Difco bactoagar |
| (7) |
酵素連結免疫分析(ELISA)試劑:
| (a) |
磷酸緩衝液:
| NaCl |
(Merck) |
8.0 |
gm |
| KCl |
(Merck) |
0.2 |
gm |
| Na2HPO4.7H2O |
(Merck) |
2.17 |
gm |
| KH2PO4 |
(Merck) |
0.2 |
gm |
| 加蒸餾水至 |
|
1,000 |
mL |
以121 ℃ 15 磅 / cm2高壓滅菌20分鐘。並以T.S.A. Agar 作無菌檢定。 |
| (b) |
PBST: 100 ml PBS中加入0.1 ml Tween 80 (0.1﹪) |
| (c) |
3﹪BSB溶液:100 ml PBS中加入3gm Bovine serum albumin (Sigma) |
| (d) |
SACIgG:綿羊抗雞IgG Conjugated horseradish peroxidase (KPL) |
| (e) |
Substrate:1份0.05﹪H2O2加9份Recrystallised 5- aminosalicyclic acid (1 mg/ml 在pH6,0.02M PBS中) (Merck)。 |
|
|
| |
|
| 3. |
膠內免疫擴散(Agar gel immunodiffusion,AGID)反應
| (a) |
以8% 氯化鈉溶液配製1% Difco bactoagar,將此混合物置於沸騰的水槽。 |
| (b) |
吸取4ml的洋菜明膠溶液在7.5x2.5cm顯微鏡載玻片上待其凝固。 |
| (c) |
在洋菜明膠上用鑿孔器進行挖孔,孔之直徑為5mm,間距為2mm,以吸引針吸去洋菜明膠塊。 |
| (d) |
測試血清加於上排及下排的孔洞中,標準陽性血清及抗原則間隔置於中間列(如圖例)。 |
| (e) |
將載玻片放在玻璃潮溼培養皿37℃下作用24小時後,在暗室利用燈光進行結果沉降線判讀。
 |
|
| |
|
| 4. |
酵素連結免疫分析(ELISA):
| (a) |
CEF或DEF培養在100mm平板上,接種MDV並產生75﹪以上CPE時,以Trypsin消化離心後,懸浮於磷酸緩衝液馬上使用或將細胞懸浮於10﹪胎牛血清及10﹪DMSO的組織培養液內,保存於液態氮中備用。 |
| (b) |
液氮保存細胞使用前先用PBS洗兩次,以便除去DMSO,最後在懸浮於PBS中。 |
| (c) |
平底96孔塑膠微量盤,盤底包覆MDV感染的CEF或DEF細胞,每孔包覆5x104/0.1ml PBS感染細胞。測試盤離心1000rpm 10分鐘,棄除上層液,在室溫中讓細胞乾燥。 |
| (d) |
包覆抗原的盤子用透明寬膠帶封緊,可以存放4℃或-20℃下至少三個月。 |
| (e) |
盤子用含0.1﹪Tween 80之PBS (PBST)洗3次。 |
| (f) |
待測之配對血清、陽性、陰性血清以3﹪Bovine serum albumin稀釋,放入測試盤中。 |
| (g) |
37℃ 1小時感作,PBS洗1次。 |
| (h) |
綿羊抗雞IgG Conjugated horseradish peroxidase 以稀釋液稀釋1:3200後,每孔加100μl。 |
| (i) |
37℃感作1小時後,以洗液洗4次。 |
| (j) |
每孔加入100μSubstrate (1份0.05﹪H2O2加9份Recrystallised 5- aminosalicyclic acid (Merck)(1 mg/ml 在pH6,0.02M PBS中))。 |
| (k) |
室溫30分鐘後,在490nm波長ELISA reader (Titertek Multiscan)判讀OD值。 |
| (l) |
ELISA reader設定重複讀3次,血清稀釋1:400者吸光度為0.2單位或更高則判定為陽性,抗體力價為吸光度為0.2單位之血清稀釋倍數的反比。 |
|
|
| |
|
| 1. |
動物傳染病診斷標準。雲林縣家畜疾病防治所彙編。 |
| 2. |
禽病檢查手冊。宋華聰、林茂勇編校。玉萱圖書出版社。1995。 |
| 3. |
Manual of Standards for Diagnostic Tests and Vaccines. Office International des Epizooties, World Organisation for Animal Health. 1997. |
|
| |
| 1. |
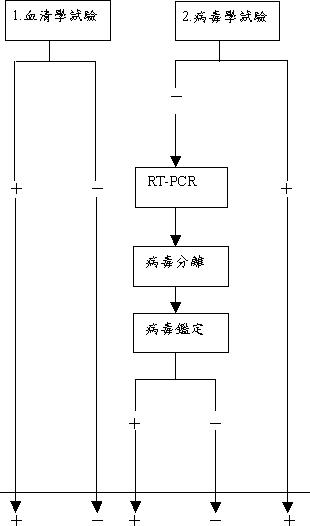
血清學試驗
方法:AGP |
| 2. |
病理學檢查:組織病變明顯病變者直接診斷,不明顯者進行病毒學試驗 |
| 3. |
病毒學試驗
|
| |
方法:接種於10-12日齡雞胚胎、已形成單層細胞之BHK-21、VERO細胞等株化細胞。
| A. |
RT-PCR陽性檢體需進行定序 |
| B. |
病材白血球層、腫瘤臟器、毛囊尖端接種CK或DEF。 |
| C. |
病毒鑑定:同居感染試驗、IF、TEM、PCR。 |
|
|