雞傳染性支氣管炎
- 內容
雞傳染性支氣管炎病毒分離及鑑定標準操作程序(以下簡稱本標準)所制定之內容係提供實驗室處理相關病材、操作病毒之各種生物活性及診斷鑑定時所必須之程序,以確保實驗室操作人員之安全性,及維持對本病診斷鑑定之精確性與快速性。目的 名詞定義 1. 雞傳染性支氣管炎: 雞傳染性支氣管炎(IB)是一種引起雞急性呼吸症狀的傳染性疾病,IB病毒感染雞隻亦會造成慢性或急性的腎炎,有時亦會造成蛋雞產蛋的障礙。當呼吸道有其他病原存在時,則IB病毒對呼吸道的病害性會加劇。本病之臨床症狀顯著,但依據此無法診斷為IB,必須分離或利用血清學的方清証實有IB病毒感染,方能証實雞罹患IB。臺灣在1958年即有呼吸道型IB的病例報告,待1964年證實IB在臺灣發生及分離該病毒,1968年迄至今在臺灣證實有腎炎型病例之發生, 目前腎炎型仍舊肆虐本省雞群,本病臨床上依其致病性可分為呼吸道型、生殖道型及腎炎型。 2. 雞傳染性支氣管炎病毒: 雞傳染性支氣管炎病毒是屬於冠狀病毒科(Coronaviridae)之第三群。IB病毒株之分型主要以病毒中和試驗與血球凝集抑制試驗來鑑別血清型。在臺灣發生之IB所分離獲得之病毒株,目前依IB病毒核酸序列分析之樹狀圖比對,證實本土型IB有臺灣I型及臺灣II型。 設施及材料 1. 實驗室:符合國家安全標準1級及2級實驗室 2. 離心機:KOKUSAN, H-103N 3. 桌上型離心機:KM-15200, KUBOTA 4. 鐵胃:STOMACHE80 5. 離心管:50 mL及15 mL容量底部V字型,微量離心管 6. 紗布塊及細紗網 7. 血球震盪器 8. 微量天平及平衡器 9. 96孔微量測定盤(V字型) 10. 1日齡與6週齡SPF(specific pathogen free)雞(本所動物用藥品檢定分所) 11. 注射針(0.5 mL、1 mL、5 mL、10 mL及20 mL容量注射針筒,含針) 12. 9-11日齡SPF雞胚胎蛋(本所動物用藥品檢定分所) 13. 8爪及12爪微量分注器及單爪微量吸管(100 μL) 14. 外科剪刀、鑷子及外科手術刀 15. 檢蛋器與孵卵器 16. 強碘酊:7 g 游離碘、5 g 碘化鉀及100 mL 85%乙醇配製而成 17. 70%酒精與酒精棉 18. 滅菌生理鹽水(0.85%) 19. 磷酸緩衝溶液(pH 7.0~7.4):0.5 M NaCl、0.5 M Na2HPO4、1.0 M NaH2PO4 加蒸餾水至總容量1000 mL(滅菌後備用) 20. 1% 雞紅血球懸浮液(由滅菌生理鹽水配製而成) 21. Alsver's solution 22. 瓊膠(Nobel agar, Difco) 23. RT-PCR試劑與核酸萃取相關試劑:
Trizol solution、chloroform(Sigma)、isopropanol(Sigama)、 75% 乙醇及DEPC水(Merck)PCR反應試劑:dNTP、Prozyme buffer、Rnasin、AMVTranscriptase、primer、Prozyme(DNA polymerase)及Template RNA24. 酵素連接免疫吸附法相關試劑(IIDEX)
已被覆IBV抗原測定盤
10mL IBV陽性對照血清
10mL正常對照血清
10mL山羊抗雞之免疫球蛋白(IgG,HtL)過氧化氫脢結合物溶液
40mL稀釋緩衝溶液(Dilution buffer)
10mL ABTS過氧化氫脢基質溶液
去離子蒸餾水
2.5mL 5×停止液(1:5方式稀釋為操作液)
20mL 20×洗滌液(1:20方式稀釋為操作液)25. 酵素連接免疫吸附法相關設備
1-20mL微量分注器
0.2mL、1.0mL及5.0mL吸管
8爪或12爪的微量分注器
未被覆抗原抗體之96孔微量測定盤
96孔盤分光判讀器
96孔盤洗滌盤26. 螢光二次抗體 臺灣腎炎型雞傳染性支氣管炎之臨床症狀與病理變化 1. 臨床症狀 (1) 雞群若罹患腎炎型IB時會出現中度或輕度呼吸症狀後,隨即產生腎炎及尿毒症。尤其在臨床上可發現病雞畏縮於雞舍一角、羽毛零亂及脫水。 (2) 病雞會排出大量水樣便,糞便中含有大量的尿酸鹽,此時陸續會有死亡病雞,其死亡率會伴隨周圍環境氣溫降低或雞舍通風不良而增加。 (3) 腎炎型之IB毒株常造成腎臟腫大,腎小管及輸尿管尿酸炎沉積結晶。 2. 病理變化 (1) 罹患腎炎型IB垂死或死亡病雞會有明顯脫水現象,其腎臟外觀出現腫大,腎小管明顯擴張與尿酸鹽沉積。 (2) 腎炎型IB之組織病理變化主要分為二種,其一是慢性進行性腎炎之病變包括腎小管上皮細胞變性、壞死與再生,腎髓質部間質有淋巴球浸潤、集尿管出現擴張、淋巴球圍管現象及尿酸鹽沉著。另一是慢性非活動性腎炎包括腎皮質部與髓質部均有淋巴球浸潤,集尿管擴張及淋巴球圍管現象,尿酸鹽沉積及其他漿細胞與巨細胞之浸潤。 (3) 呼道型之IB會造成氣管絨毛脫落及上皮增增生、脫落、充血、炎症滲出物、及大量單核球浸潤黏膜下層。氣囊會出現上皮細胞變形、水腫、纖維性滲出物出現及淋巴球與異嗜球增加、及上皮再生。 (4) 有些IB毒株會造成輸卵管的病變:如輸卵管上皮細胞的壞死、脫落、輸卵管壁水腫及淋巴球浸潤。 初代分離培養病材採集與處理 1. 病材採樣 (1) 一般疑似IB病例採樣,可以在產生急性呼吸道病例時,採取氣管拭子或禽體的氣管和肺組織,並添加入磷酸緩衝溶液 (含penicillin 10,000 IU/mL,streptomycin 10 mg/mL及amphotericin 250 IU/mL), 迅即移置於冰凍中。若病雞出現腎炎或產蛋障礙時,儘可能採取腎臟或輸卵管等臟器,另外亦可採取大腸之盲腸扁桃或糞便等試材亦可獲得高的病毒分離率。 (2) 試驗材料可利用無菌並含抗生素的培養液研製成20% (w/v)組織懸浮液,置於無菌袋中經鐵胃擊碎臟器試材,並置於15 mL無菌離心管中。 (3) 經3000 g離心10分鐘後取上清液,再直接接種於雞胚胎或氣管環細胞。 2. 病毒分離與增殖 (1) 取0.1~0.2 mL試材上清液接種於9-11日齡雞SPF胚胎尿囊腔,置於孵蛋器中,接種後每天觀察,並淘汰丟棄接種後24小時內死亡的雞胚胎,收集接種後2-7日死亡雞胚胎尿囊液置於零下60 ℃或以下保存。 (2) 接種5-7日後收集未死亡雞胚胎尿囊液,並加入1/5或1/10量的含抗生素溶液,並繼續接種下一個雞胚胎蛋。野外病毒株經二次或三次盲目繼代接種即可導致雞胚胎死亡或雞胚胎畸型。同樣採集此具感染性的尿囊液。 (3) 氣管培養可以由20日齡SPF之雞胚胎製備,並可將試材直接接種於此培養的氣管中以達分離IB病毒之目的。 (4) 利用組織切割機可以製備大量橫切的氣管環,使每一個氣管環大約0.5-1mm的厚度,並加入細胞維持培養液(Eagle's N-2-hydroxyethyl piperazine N'-2-ethanesulphonic acid ,HEPES),在37℃中培養,則在病毒感染後24-48小時氣管上皮細胞會產生纖毛不動的現象。 病毒鑑定與血清學試驗 1. 1%雞紅血球懸浮液之製備流程 (1) 由3週齡以下之SPF雞採下之全血與2:1體積之比例與Alsver's solution混合,以阻止血液凝固,輕輕充份混合。 (2) 經細紗網過濾,以去除血液中大的凝塊,再加適量的滅菌生理鹽水,充份混合。 (3) 經1000 rpm 離心10分鐘,倒掉上清液,再加入適量滅菌生理鹽水,輕輕懸浮紅血球。 (4) 重復前述步驟,1000 rpm 離心10分鐘,倒掉上清液,再加入適量滅菌生理鹽水,輕輕懸浮紅血球。 (5) 經1500 rpm離心15分鐘,倒掉上清液,將血球調成1%雞紅血球懸浮液。 (6) 將製備好之1%雞紅血球懸浮液放置於4 ℃冰箱中。 2. 血球凝集試驗: (1) 抗原的製備:
具病毒尿囊液經30,000g離心3小時,倒棄上清液,並將沉澱物 (pellet) 以100倍之濃縮液(0.01M Tris HC1 buffer,pH 6.5)再懸浮。(2) IB病毒必須經酵素處理血球凝集素(Haemagglutinin,HA)才具有活性,病毒懸浮液與等量磷酸脂酶 C 第一型酵素phospholipase C type I enzyme)混合,使其終濃度為每毫升含有1單位(unit)的酵素。此種病毒/磷酸脂酶之混合物靜置於37℃作用2小時。 3. 血球凝集試驗(Haemagglutination test,HA)(附錄一) (1) 分注0.025 mL磷酸緩衝溶液(phosphate buffered isotonic saline , PBS , pH 7.0-7.4)於96孔力價測定盤(v字型底)。 (2) 加0.025 mL病毒液入測定盤之第二孔,為準確測定HA的含量,則病毒液先稀釋一濃度如1/3,1/4,1/5,或1/6等,再進行極限稀釋。 (3) 以0.025 mL的病毒量在測定盤上進行連續2倍稀釋至每一孔。 (4) 每一孔再加入0.025 mL PBS溶液。 (5) 最後每一孔加入0.025 mL 1%雞紅血球懸浮液。 (6) 將測定盤置於震盪器輕微震盪,並靜置40分鐘,對照組之紅血球必須沉降至v字型底部。 (7) 將測定盤傾斜以判定HA,並觀察RBC是否有眼淚狀的流出物,若沒有眼淚樣的流出物則可判讀到最高稀釋倍數的HA,此表示為1個HA單位(HA unit,HAU),且從最初的稀釋範圍而準確計算出含多少HA單位。 4. 血球凝集抑制試驗(Haemagglutination inhibition test,HI)(附錄二) (1) 取0.025 mL的PBS分注測定盤之每一孔(V-字型底)。 (2) 加0.025 mL血清入測定盤第一孔。並經 2倍連續稀釋每一孔為0.025 mL。 (3) 每一孔再加入4HAU的病毒抗原輕微震盪,並靜置30分鐘。 (4) 每孔再加入0.025 mL 1%雞紅血球懸浮液輕微振盪後靜置40分鐘,且對照組之正常1%雞紅血球懸浮液應可沉降至V字型底部。 (5) HI的力價是指血清最高稀釋濃度可以完全抑制4HAU的抗原。由傾斜觀察測定盤之凝及試驗會更精確。 (6) 對照組的孔僅含有0.025毫升1%的雞紅血球懸浮液和0.05 mL的PBS同樣有眼淚樣的流狀物。陰性對照組血清其力價不可大於4倍,且陽性對照組血清必須檢測出預估之HI力價。 5. 病毒中和試驗(Virus neutralisation;VN) (1) 在進行病毒中和試驗前所有的血清必須經56℃加熱30分鐘,病毒再與檢測血清充份混合在室溫中感作30至60分鐘,並接種於雞胚胎或感染組織培養細胞,但是仍以組織培養細胞系統等方法來檢測抗體較佳。 (2) 有二種估測中和抗體的方法,其一是血清濃度固定及各稀釋濃度病毒液(α-method;α法),另一是病毒感染力價固定及各稀釋血清濃度(β-method;β法)。 (3) 在α法檢測中,經雞胚胎馴化病毒十倍連續稀釋濃度與固定抗血清濃度(約1/5)充份混合並接種5至10個雞胚胎蛋,同時進行病毒單獨感染力價測定,終點測定(End-points)以Karber或Reed &Muench 法來估測。中和試驗指數(Neutralisation index , NI)表示抗血清與病毒感染力價之log10 間的差異值結果。NI值在同源性的病毒/血清混合物可達4.5-7.0。此NI值若小於1.5時為非特異性反應,但是異源性病毒時,則產生的NI值亦必然小於1.5。 (4) β-法亦更廣泛使用於利用雞胚胎來測定中和試驗,以達檢測抗體分析之目的。本法主要是抗血清2倍或4倍連續稀釋濃度和0.05mL和0.1 mL的固定100 EID50 (50% egg-infective doses)感染力價病毒液作用混合,再將混合物經尿囊腔接種5-10個雞胚胎蛋,亦同時進行病毒感染力價測定,以達証實病毒/血清混合物中的病毒感染力價維持在101.5至102.5 EID50之間,血清力價之終點測定以Kaber 或Reed & Muench來估測之,但以log2 稀釋濃度表示之。此種固定病毒濃度而血清不同濃度的方法也曾在氣管臟器細胞培養進行中和試驗分析,並每一血清稀釋濃度同時加入5個培養細胞。根據Reed & Muench 法估測抗體力價的結果中,病毒感染力價以50% median ciliostatic dose per unit volume(log10 CD50)表示,血清中和力價再以log2稀釋濃度表示。 6. 酵素連接免疫吸附法: (1) 取出96孔檢測盤(已被覆IBV抗原) (2) 取稀釋緩衝溶液分注到每一孔,每一孔加入50μL量;A1,A3,及H11孔之測定盤分別置入50 μL之陰性對照血清。其他90孔分別加入50 μL檢測血清及陰性血清感作,置放於室溫感作30分鐘。 (3) 檢測盤之洗滌,倒棄(2)之感作液,每孔加300 μL洗滌液(Washing solution )。 (4) Soak 3分鐘,並倒置檢測盤,以完全去除殘留之洗滌液。 (5) 重覆(3)(4)之步驟2次以上,以去除檢測盤非特異性的物質。 (6) 檢測盤每孔加入100μL已稀釋之抗雞IgG過氧化氫酵素結合物, (7) 並在室溫中感作30分鐘 (8) 倒棄洗滌液,並加入洗滌液300 μL。 (9) Soak3分鐘,並重覆洗滌過程(7)。 (10) 倒棄洗滌液,並加入100μL基質溶液(substrate solution),並在室溫中感作15分鐘。 (11) 每孔加入100 μL停止液(stop solution),以終止反應,以備進行判讀。 (12) 判讀以405-410 nm波長之ELISA判讀器進行分析,紀錄A1,A3及H11之陽性對照血液之平均吸光值。紀錄A2,H10 和 H12之陰性對照血清之平均吸光值,計算檢測血清陽性之吸光值 (13) SP(Sample to positive)=(檢測血清吸光值-平均正常陰性血清對照組吸光值)/(平均陽性血清對照組吸光值-平均陰性血清對照組) 7. 反轉錄聚合酶鏈反應(reverse transcriptase polymerase chain reaction;RT-PCR) (1) 病毒RNA萃取 (a) 病材之臟器組織作成10倍乳劑。 取100μL病材乳劑加入1 mL Trizol萃取液充份混合30秒並靜置室溫5分鐘。 (b) 加入200 μL 氯仿 (chloroform) 以手上下倒置混合15秒後靜置室溫3分鐘,置於4 ℃下12,000 g離心15分鐘。 (c) 取上清液與等量isopropanol充分混合靜置室溫10分鐘,再置於4 ℃下12,000 rpm離心15分鐘。 (d) 倒棄上清液加入1 mL 75% 乙醇後於4 ℃ 下14,000 g離心5分鐘後去上清液。 (e) 置56 ℃烘箱或真空乾燥去除水份後加入60至80μL DEPC (diethylpyrocarbonate) 處理水溶解,迅即進行RT-PCR過程。 (2) 以反轉錄聚合酶鏈反應增幅核酸 (a) 引子(primer)設定:參閱GeneBank設定S1 gene特異性引子。 (b) 反轉錄聚合酶鏈反應(RT-PCR)操作過程:
首先配製PCR反應液包括 dNTP (dATP、dTTP、dGTP、dCTP mixtures 1.25 mM) 16 μL、 10 倍 Dynazyme buffer 10 μL, RNasin (40 U/μL) 0.4 μL、 AMV transcriptase (8 U/μL) 0.3 μl、 primer 1 μL (0.5μg/μL)、 DNA polymerase 1μL及 template RNA (即樣品 RNA) 13 μL, 加無菌蒸餾水至100 μL為最終反應體積。以溫度循環控制器中進行PCR,其反應條件為42 ℃ 40分鐘單-循環。94 ℃ 40秒,45 ℃ 1分鐘,72 ℃ 1分鐘進行35個循環。72 ℃延長7分鐘。(c) RT-PCR產物電泳分析:
取RT-PCR產物2μl之loading dye混合後,灌入2%洋菜膠中進行電泳分析。在迷你電泳槽(Mupid-II, Cosmo)中加入TAE buffer (40 mM Tris-acetate, 1mM EDTA),以100伏特電壓進行電泳25分鐘,並置於UV燈下觀察,以Polaroid type 667相紙顯影記錄結果。8. 瓊膠免疫擴散法(agar gel immunodiffusion test, AGID) (1) 標準抗原的製備 (a) 將IB疫苗株或野外病毒株分別接種於10日齡SPF雞胚尿囊腔中,增殖至48小時後冰存於4 ℃中10小時以上,抽取含病毒尿囊液置於零下70 ℃,以備純化病毒之需。 (b) 將前步驟收取之含病毒尿囊液在4 ℃下2,000 g 離心10分鐘,並取含病毒上清液。再經超高速離心機(Hitachi, )在4 ℃下28,000 rpm離心4小時,取病毒沉澱物並以TEN緩衝溶液100倍濃縮。 (c) 將濃縮之病毒液放置於15-50%蔗糖梯度溶液中,重複前述離心步驟,並取比重在1.6之病毒層,再以適量TEN緩衝溶液懸浮及再經不超高速離心將病讀沉澱下來,並將純化之病毒保存於零下70 ℃中備用。 (2) 兔抗IBV標準血血清之製備 (a) 將6.(1)之標準抗原分別與佛氏完全佐劑(complete freund's adjuvant, sigma)及不完全佐劑(incomplete freund's adjuvant, sigma),以1:1比例混合(以三通式連接管混合均勻),並置於4 ℃下備用。 (b) 準備1.5公斤重之紐西蘭兔,免疫接種前先採血以備血清學試驗之陰性對照。先取完全佐劑劑型之IBV 1 mL接種免疫免子(皮下注射),經第一次免疫兩週後,使用不完全佐劑劑型之IBV 1 mL接種免疫兔子(皮下注射)一次,再經兩週後以1 mL濃縮之IB病毒液進行兔子靜脈注射。 (c) 靜脈注射IB病毒液兩週後進行兔子之心臟採血並分離血清,將血清放製於零下70 ℃中備用。 (3) 瓊膠平皿之製備 (a) 取 1 克瓊膠(Difco, Nobel agar)與8克NaCl溶解於100 mL二次蒸餾水中,先經100 ℃水浴煮沸充份溶解。 (b) 再經高溫高壓滅菌10分鐘後及待冷卻至45 ℃左右的溫度,分裝於直徑約9公分之塑膠平皿中(約18 mL),待冷卻後放於4 ℃冰箱中備用。 (4) 瓊膠免疫擴散法 (a) 將已製備好之AGID test之平皿進行打孔,並去除孔中之凝瓊膠,每一組共7孔,周圍6孔,中央1孔,呈六角形同心圓排列。每一孔之直徑為 5 mm,間距 3 mm。 (b) 測定抗體或抗原時,周圍孔分別放置標準抗原或標準抗體,所有孔放入40 μL的量,並放入保有濕度之盒子中。 (c) 放置在室溫中,待24至72小時判讀,以觀察沉澱線之有無。 9. 間接螢光抗體法 (1) 以10 m.o.i IBV病毒感染力價感染96孔細胞培養皿內未長滿的CK(chicken kidney cell)初代細胞。 (2) 感染後24小時左右細胞開始出現細胞病變,倒掉病毒液並直接加入冰冷的固定液(丙酮:甲醇:水=4:4:2),在4 ℃下固定10分鐘後倒掉固定液,室溫下任其風乾,封入塑膠袋中並保存在零下70 ℃備用。 (3) 無感染IBV之BHK細胞,處理同上步驟。 (4) 檢測IBV抗體時,每孔加入100 μL檢測血清,37 ℃下感作90分鐘,以PBS-Tween溶液清洗三次,在加入以1% BSA溶液稀釋之FITC標示的二次抗體,37 ℃下感作90分鐘後,再以PBS-Tween溶液清洗四次,每次震盪5分鐘,倒乾清洗液後即可在螢光顯微鏡下觀察,並記錄之。 病毒核酸序列分析 1. 病毒RNA萃取 (1) 病材之臟器組織作成10倍孔劑。取100 uL病材孔劑加入1mL Trizol萃取液充份混合30秒並靜置室溫5分鐘。 (2) 加入200 uL氯仿(chloroform)以手上下倒置混合15秒後靜置室溫3分鐘,置於4℃下12,000 rpm離心15分鐘。 (3) 取上清液與等量isopropanol充分混合靜置室溫10分鐘再置於4℃下12,000 rpm離心15分鐘。 (4) 倒棄上清液加入1 mL 75﹪乙醇後於4℃下14,000 g 離心5分鐘後去上清液。 (5) 置56℃烘箱或真空乾燥去除水份後加入60至80 uL DEPC (diethypyrocarbonate) 處理水溶解,迅即進行RT-PCR過程。 2. 病毒核酸之增幅 (1) 引子 (primer) 設定:參閱GeneBank設定F gene特異性引子。 (2) 反轉錄聚合酶鏈反應 ( RT-PCR) 操作過程: (a) 首先配製PCR反應液包括dNTP(dATP、dTTP、dGTP、dCPT mixtures 1.25 mM)16uL、10倍Dynazyme buffer 10 uL,RNasin(40 U/ uL)0.4 uL、AMV transcriptase(8 U/ uL)0.3 uL、primer 1 uL(0.5ug/ uL)、DNA polymerase 1 uL 及 template RNA(即樣品RNA)13 uL, 加無菌蒸餾水至100 uL為最終反應體積。 (b) 以溫度循環控制器中進行PCR,其反應條件為42℃ 40分鐘單一循環。94℃ 40秒,45℃ 1 分鐘,72℃ 1分鐘進行35循環。72℃延長7分鐘。 3. 核酸序列分析 (1) 將八-2.步驟合成之PCR產物進行自動核酸序列分析、分析融合蛋白氨基酸序列,第113-116個位置若具有3個以上鹼性氨基酸且第117個位置為phenylalanine之氨基酸即判定為雞傳染性支氣管炎。 (2) RT-PCR產物電泳分析:取RT-PCR產物2ul之loading dye混合後,灌入2﹪洋菜膠中進行電泳分析。在迷你電泳槽 ( Mupid-II,Cosmo) 中加庄TAE buffer (40 mM Tris-acetate, 1mM EDTA),以100伏特電壓進行電泳25分鐘,並置於UV燈下觀察,以Polaroid type 667相紙顯影記錄結果。 酵素連接免疫吸附法 1. 取出96孔檢測盤(已被覆NDV抗原) 2. 取稀釋緩衝溶液分注到每一孔,每一孔加入50 uL量A1,A3,及H11孔之測定盤分別置入50 uL檢測血清及陰性血清感作,置放於室溫感作30分鐘。 3. 檢測盤之洗滌,倒棄 (2) 之感作液,每孔加300 uL洗滌液 (Washing solution)。 4. Soak 3分鐘,並倒置檢測盤,以完全去除殘留之洗滌液。 5. 重覆 (4) 之步驟2次以上,以去除檢測盤非特異性的物質。 6. 檢測盤每孔加入100 uL已稀釋之抗雞IgG過氧化氫酵素結合物,並在室溫中感作30分鐘。 7. 倒棄洗滌液,並加入洗滌液300 uL。 8. Soak 3分鐘,並重複洗滌過程2. (6) (7)。 9. 倒棄洗滌液,並加入100 uL基質溶液 (substrate solution),並在室溫中感作15分鐘。 10. 每孔加入100 uL停止液 (stop solution),以終止反應以備進行判讀。 11. 判讀以405-410 nm波長之ELISA判讀器進行分析,紀錄A1,A3及H11之陽性對照血液之平均吸光值。紀錄A2,H10和H12之陰性對照血清之平均吸光值。 12. 計算檢測血清陽性之吸光值
SP(Sample to positive)=(檢測血清吸光值-平均正常陰性血清對照組吸光值)/(平均陽性血清對照組吸光值-平均陰性血清對照組)附錄 附錄一、血球凝集試驗

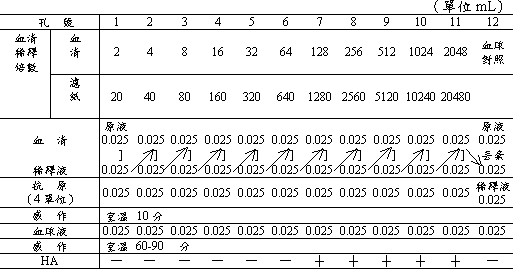
附錄二、血球凝集抑制(HI)試驗